Alt om Batterier » Forstå teknologien nemt med vores Guide
Batterier kan anvendes i mange forskellige produkter, lige fra legetøj, cykel- samt lommelygter, LED fyrfadslys, postkort med lyd, armbåndsure og utallige andre ting.
Faktisk ved de færreste hvordan batterier virker, og hvad de består af.
Jeg vil i dette indlæg fortælle dig alt om batterier, så du kan forstå teknologien bag.
Hvordan virker batterier? Et batteri er en enhed som oplagrer elektricitet i form af kemisk energi som så konverteres den kemiske energi til elektricitet. Der findes forskellige batterityper som bruger forskellige kemiske reaktioner til at oplagre energien, men konceptet er ens for alle typer.
Hvis du har lyst til at lære meget mere om batterier, om hvordan de virker og hvad de består af, så læs med herunder.
Indholdsfortegnelse
Hvad består batterier af?
Materialet der befinder sig i et batteri kan variere alt efter hvilket batteri der er tale om.
For at simplificere dette, tager jeg udgangspunkt i de klassiske Alkaline batterier som du typisk bruger til f.eks. din fjernbetjening.
Alkaline batterier består af flere forskellige lag, plastik for det visuelle, og en negativ samt positiv ladning.
Det du ser udefra, er et lag af plastik som bliver brugt til at tilføje det visuelle til batteriet samt 2 ender i metal, en med positiv og en med negativ ladning.
På indpakningen finder du typisk producentens logo, navn på batteritypen og diverse vigtige informationer såsom volt, kapacitet i mAH samt et plus og minus.
På batteriet er der 2 poler, én negativ og én positiv pol, den positive pol forbindes til katoden, og den negative til anoden.
Katoden og anoden er 2 lag inde i batteriet, som bliver brugt til at oplagre og udgive elektricitet.
Jeg vil fortælle mere om dette længere nede i indlægget,hvor jeg forklarer om indmaden i batteriet.
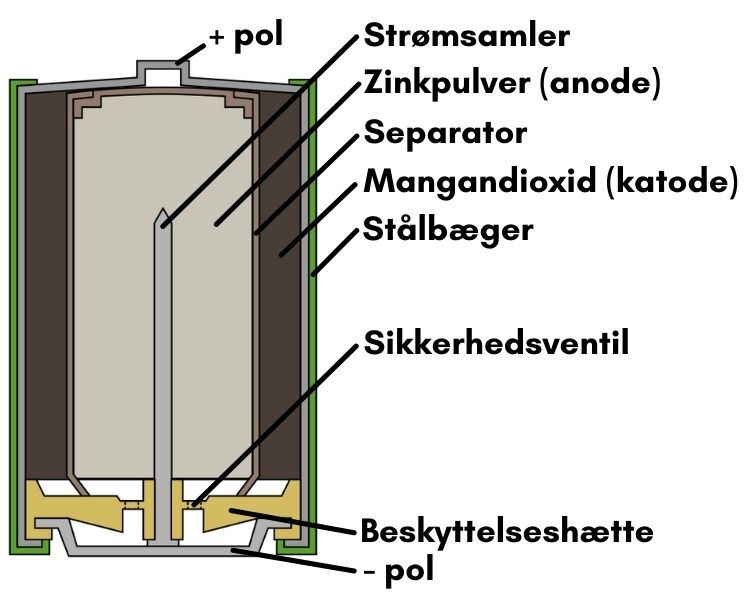
Inde I batteriet
Under plastik laget er der et lag af stål, som holder indmaden i batteriet på plads, hvilket beskytter for eventuelle skader og forhindrer ting såsom luft og vand i at trænge ind i batteriet.
Indmaden af batteriet består af flere forskellige lag, som er med til at oplagre den kemiske energi og konvertere energien til elektricitet.
Det yderste lag af indmaden kaldes en katode.
I Alkaline batterier bruges der mangandioxid blandet med kulpulver som materiale i katoden.
Kulpulveret tilføjes for at øge katodens ledningsevne og energi tæthed.
Under katoden er der en separator, som adskiller katoden fra anoden, og dermed isolerer de 2 lag så de ikke har direkte kontakt.
Formålet med at isolere kontakten mellem katoden og anoden er, at forøge batteriets levetid når det ikke bliver brugt. Hvis der ikke er en separator i batteriet, vil det kortslutte.
I separatoren er der små mikroskopiske huller, som gør at ioner kan trænge gennem.
Under produktionen af Alkaline batterier bliver der spøjtet en elektrolyt på separatoren, som så bliver absorberet, og ligger som et lag mellem katoden og anoden.
På indersiden af separatoren befinder anoden sig. Alkaline batterier bruger Zink i pulverform som materiale i anoden.
Zink bliver brugt i pulverform for at forøge overfladearealet, hvilket forøger elektronstrøm og mindsker den interne modstand.
Strømsamleren sidder inde midt i batteriet, og består af brass, hvilket bruges til at opfange elektronerne og sende strømmen ud.
Under strømsamleren er der en beskyttelseshætte, som sidder lige bag ved den negative pol.
Beskyttelseshætten er med til at sørge for at katoden og anoden er isoleret fra hinanden, for at undgå kontakt og dermed kortslutning.
Nogle batterityper vil bruge andre materialer eller have en lidt anden opstilling end Alkaline batterier, men konceptet er det samme.
Alle batterier vil have en katode, anode samt elektrolyt, og hvilket materiale der anvendes kan variere efter hvilken type der er tale om.
Alkaline batterier kaldes eksempelvis Alkaline fordi de bruger noget der hedder en Alkaline elektrolyt.
Hvordan virker batterier?
For at forstå hvordan batterier virker skal du først og fremmest have en generel forståelse af hvordan elektricitet fungerer.
Elektricitet er en betegnelse for et kredsløb af elektroner.
Elektronerne vil altid søge tilbage til kilden, og udnytter enhver mulighed for at komme tilbage til kilden igen.
Det er derfor elektricitet altid vil kræve 2 poler, en der afgiver elektroner, og en der modtager elektroner.
Ved at sætte ting, eksempelvis en lampe, i midten af kredsløbet, vil elektronerne skulle ind gennem lampen før de kommer tilbage til kilden, og derved give lampen elektricitet.
Oftest vil batterier bruger DC (Direct Current) strøm, hvilket er strøm hvor elektronerne konstant bevæger sig i samme retning.
I batterier afgives elektronerne fra den negative pol, og modtages af den positive pol når de vender tilbage til kilden.
Hvad sker der inde i batteriet?
At forstå hvad der sker inde i et batteri kan være lidt forvirrende, hvis ikke du har en grundviden inden for kemi og kemiske reaktioner.
Alle atomer er bygget op af en kombination af protoner, neutroner og elektroner.
Neutroner har en neutral ladning, protoner har en positiv ladning og elektroner har en negativ ladning.
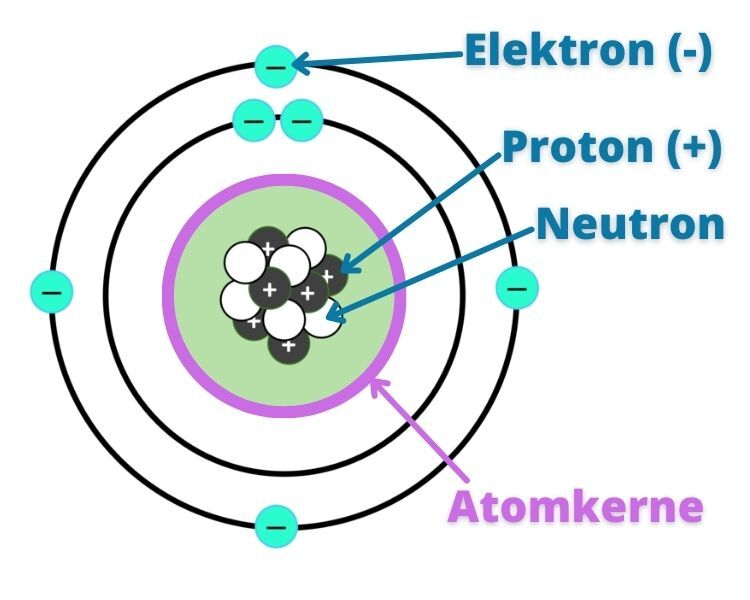
I billedet herover kan du se hvordan et atom er opbygget.
Protoner og neutroner befinder sig inde i atomkernen, og elektronerne cirkulerer rundt om atomets kerne.
Hvis et atom har lige mange protoner og elektroner er der tale om et neutralt atom.
Hvis et atom har flere elektroner end protoner, er atomet negativt ladet og omvendt vil en atom som har flere protoner end elektroner have en positiv ladning.
Et atom som har en positiv eller negativ ladning kaldes for en ion, og disse ioner er hvad du finder inde i et batteri.
Ioner vil helst have en neutral ladning, og søger efter andre ioner som de kan forbindes med for at opnå den neutrale ladning.
Disse ionbindinger er præcis hvad der sker inde i et batteri.
En ion kan både opdele eller samle flere forskellige atomer for at opnå den neutrale ladning, og i processen kan ionen afgive nogle elektroner.
Katoden, anoden og elektrolytterne bliver brugt til at skabe ionforbindelser og afgive elektroner som så opfanges af strømsamleren.
Derefter bliver de afgivne elektroner sendt ud i kredsløbet og giver strøm til den tilsluttede enhed, og vender tilbage ind i batteriet hvor elektronerne så vil bindes til ionerne igen.
Efter batteriet er blevet brugt i et stykke tid, løber anoden tør for elektroner som kan kan gives videre til katodens ioner, og derfor løber batteriet tør for strøm.
Hvordan virker genopladelige batterier?
Konceptet med genopladelige batterier er det samme som alle andre batterier, der er en katode, en anode og en elektrolyt til stede.
Et batteri som ikke kan genoplades vil løbe tør for strøm når anoden ikke har flere elektroner der kan frigives, og katoden har opfanget alle elektronerne.
Et genopladeligt batteri er i stand til at sende elektronerne tilbage til anoden så hele den interne proces kan gentages.
Ved hjælp af elektricitet fra en ekstern strømkilde, kan et genopladeligt batteri vende kredsløbet så elektronerne der nu befinder sig i katoden kan sendes tilbage i anoden.
På den måde kan batteriet igen sende strøm efter batteriet, eller anoden bliver opladt og klar til at afgive elektroner gennem kredsløbet igen.
Selvom et batteri er genopladeligt, vil det stadig have en begrænset levetid, da de mange repetitioner af de kemiske reaktioner vil skade metallerne i batteriet.
Et genopladeligt batteri vil derimod være mere bæredygtigt end et batteri som ikke kan genoplades, og måske holde i flere år, frem for flere timer.
Læs også: Sådan virker Solceller - (God forklaring, let at forstå)
Læs også: Alt om radiobølger » 10 Enheder med radiobølger (Oversigt)


